El tipo de selenio y la forma en la que se complementa desempeñan un papel crucial en su seguridad, biodisponibilidad y eficacia. Es esencial elegir bien la fuente de selenio
Los suplementos de selenio están disponibles en varias formas: sales minerales inorgánicas, como el selenito o el selenato de sodio; formas orgánicas, como la levadura enriquecida con selenio en la que predominan los análogos de selenoaminoácidos como la selenometionina; o selenoaminoácidos y análogos de selenoaminoácidos producidos sintéticamente. La distribución y acumulación del selenio y su forma en los tejidos animales depende en gran medida del tipo de suplemento de selenio, y la forma en que se presenta el selenio desempeña un papel crucial en su biodisponibilidad y eficacia. Las formas orgánicas de selenio son la fuente nutricional óptima, y al ser captadas por la célula, se transforman en selenointermediarios comunes para su posterior utilización y/o excreción.
Un alto contenido de SeMet no significa una alta biodisponibilidad
Existe una idea errónea en la industria de los piensos sobre el contenido total de SeMet en los productos de selenio, con la creencia de que «más es mejor». Tales argumentos carecen de base científica y, de hecho, no hay pruebas de que el aumento del nivel de SeMet equivalga a un mejor producto. Si bien el nivel de SeMet puede variar entre los productos, también es de prever que la bioaccesibilidad y la disponibilidad del SeMet que se libera por los procesos digestivos en el tracto gastrointestinal también serán diferentes. Desde el punto de vista de la investigación, lo que está cada vez más claro es que la forma en la que se presenta el selenio influirá en la estabilidad y, por tanto, en la reactividad celular de la molécula. Las formas menos estables de selenio tienen mayores propiedades toxicológicas, mientras que las de los preparados más estables son mucho menos tóxicas.
En uno de los primeros estudios, que demostró la singularidad de los productos individuales de selenio, los autores examinaron tres preparaciones comerciales diferentes de levadura enriquecida con selenio, sometiendo a cada una de ellas a una serie de extracciones secuenciales seguidas de varias digestiones enzimáticas diseñadas para liberar selenocompuestos que están asociados a varias fracciones de polisacáridos y proteínas. Posteriormente, estos compuestos se separaron y se especificaron mediante SEC-ICP MS, y se compararon las recuperaciones en las distintas fracciones de cada producto de levadura(Figura 1). Los resultados que se muestran en la Figura 1 muestran el fraccionamiento de los selenocompuestos en la levadura utilizando diferentes técnicas de extracción
Figura 1 – Fracciones de levadura asociadas al selenio (adaptado de
Encinar et al, 2003)
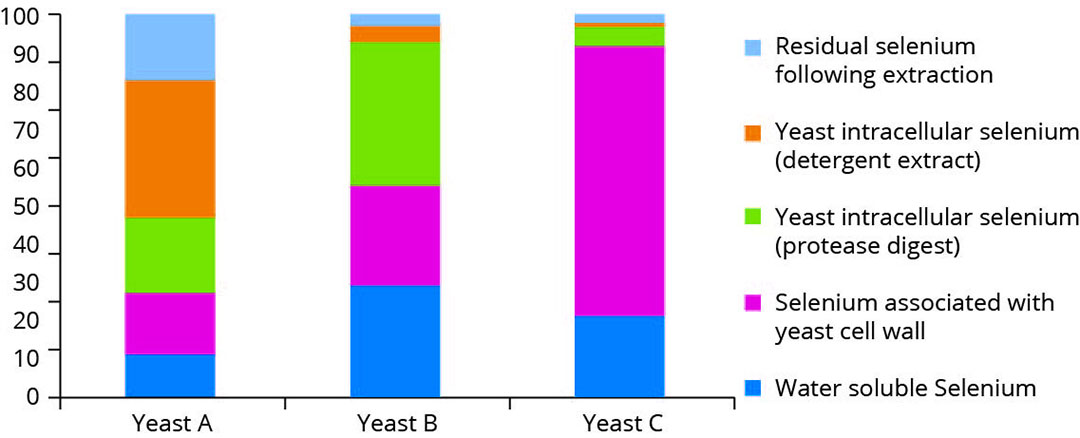
No todas las levaduras de selenio son iguales
Aunque existe una percepción muy común de que todos los preparados de levadura con selenio son iguales, no es así, y está claro que la compartimentación del selenio dentro de la levadura es totalmente diferente entre los preparados. Al igual que existen diferencias entre las cepas de levadura a nivel genético, hay diferencias fundamentales en la forma en que las levaduras distribuyen el selenio dentro de la célula
Dado que la deposición subcelular de selenio en los preparados de levadura enriquecidos con selenio es tan diferente, es razonable esperar que estos preparados también difieran en parámetros como la vida útil, la biodisponibilidad y, de hecho, la toxicología. En lugar de considerar estos productos bajo la misma luz, deben verse como preparados de selenio distintos.
Dada la naturaleza altamente regulada del uso del selenio y de los productos de selenio, se puede encontrar fácilmente mucha información en relación con áreas como la toxicidad y la estabilidad de la fuente de selenio. Este tipo de información permite a los usuarios finales tomar decisiones informadas en cuanto a la idoneidad de los productos individuales tanto para sus sistemas de producción como para su uso final.
Tabla 1 – Estabilidad de la fuente de selenio

Estabilidad de la fuente de selenio en las premezclas y los piensos
A partir de los dictámenes normativos sobre los materiales, en la Tabla 1 se destaca un examen diferencial de los datos de estabilidad disponibles sobre la levadura de selenio orgánico y las fuentes de selenio sintético, a partir del cual se pueden apreciar notables diferencias entre ellos.
Quizá lo más llamativo de las comparaciones sean las notables diferencias entre sus estabilidades en la premezcla. La inestabilidad de una de las fuentes de selenio sintético fue bastante notable, ya que la recuperación después de tres, seis y nueve meses fue del 55%, 54% y 37%, respectivamente.
El examen de la otra fuente sintética no mostró la estabilidad medida del compuesto real y, en cambio, informó de ella para una molécula variante no elenizada. Quedan otros interrogantes sobre la estabilidad de las fuentes sintéticas en los piensos compuestos y después de la granulación, ya que o bien no se han generado datos suficientes o no se ha realizado ninguna medición directa de la estabilidad.
Por el contrario, las fuentes orgánicas de levadura de selenio muestran altos niveles de estabilidad verificada en premezclas, piensos compuestos y después de la granulación, aunque se observan otras diferencias entre ellas que dependen de la fuente.
Dado el aumento de los costes de las materias primas y los aditivos, no es de extrañar que los fabricantes de premezclas y piensos presten cada vez más atención a las formulaciones y, en particular, a la estabilidad de los materiales individuales. Las posibles pérdidas debidas a las interacciones en la premezcla o como resultado del granulado son motivo de gran preocupación.
Tabla 2 – Toxicidad de la fuente de selenio y etiquetado de peligro.
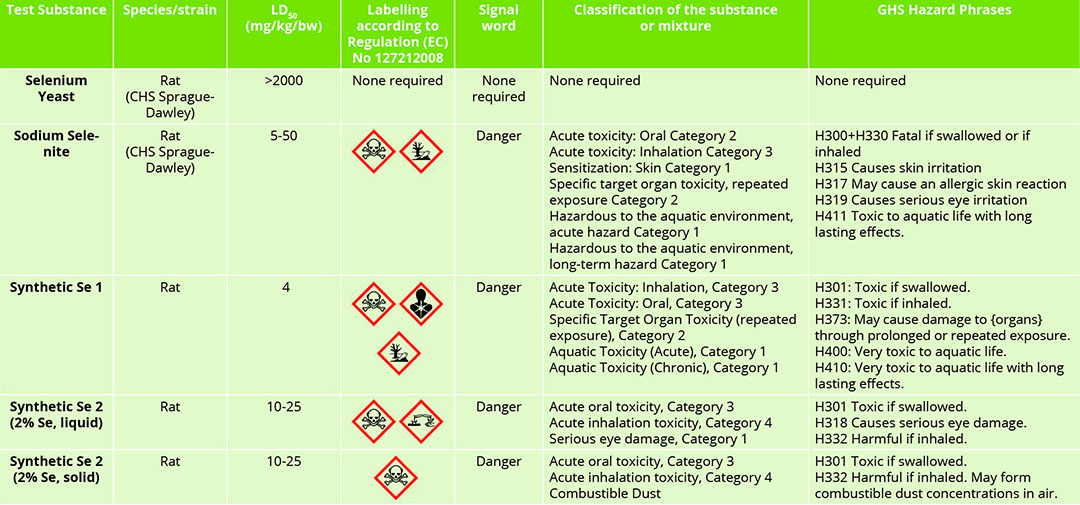
Diferencias de toxicidad entre las fuentes de selenio
La tabla 2 destaca las toxicidades diferenciales asociadas a las fuentes de selenio inorgánicas, orgánicas y de síntesis química. En estos datos destacan las notables diferencias entre las fuentes de selenio. El producto de levadura de selenio orgánico tiene relativamente pocas connotaciones negativas, si es que las tiene, asociadas a su uso.
En cambio, las fuentes de selenio inorgánico y sintético tienen atributos tóxicos claramente definidos, que son notablemente bastante similares con respecto a sus toxicidades orales agudas. También son interesantes las sutilezas asociadas a las toxicidades de las formas líquidas y sólidas de la misma fuente de selenio sintético. Está claro que, al considerar las fuentes de selenio, no se puede clasificar a todas como iguales.
Las razones de las diferencias de toxicidad
Para entender las diferencias de toxicidad entre las fuentes de selenio, puede ser útil examinar la bioquímica que hay detrás del selenio y su potencial para actuar negativamente a nivel celular.
Las propiedades prooxidantes de las fuentes de selenio, como el selenito de sodio, se originan en su conversión en seleniuro o selenoles, que se oxidan fácilmente y generan especies reactivas de oxígeno (ROS). La toxicidad del selenito está bien documentada como causada principalmente por el daño al ADN debido a la inducción de roturas de la cadena de ADN dependientes de las ROS y/o la oxidación de las bases, lo que conduce a la muerte celular apoptótica y necrótica
Investigaciones más recientes han demostrado que los selenocompuestos de libre acceso (como el selenio sintetizado químicamente) pueden tener propiedades prooxidantes, que se inician de la misma manera que el selenito de sodio, pero que pueden potenciarse aún más debido al inicio de ciclos adicionales de oxidación/reducción. En última instancia, estos ciclos redox consumen antioxidantes intracelulares como el GSH y, en consecuencia, el cofactor reductor NADPH. Estos ciclos redox inducidos por los selenocompuestos no sólo pueden provocar un desequilibrio antioxidante, sino que también pueden conducir a una producción mayor y sostenida de ROS, que pueden dañar aún más los ácidos nucleicos, las proteínas y los lípidos
Además, los selenoles oxidados catalizarán la formación de puentes disulfuro entre los tioles de bajo peso molecular y las proteínas, lo que puede provocar la inactivación o la agregación de proteínas
Estudios más recientes indican que la toxicidad de los selenocompuestos de libre acceso es el resultado de su conversión en selenocisteína, un selenoaminoácido con capacidad para mediar en el estrés proteotóxico, desempeñando así un papel en la toxicidad del selenio que hasta ahora se había subestimado
El riesgo inherente de toxicidad de la proteotoxicidad mediada por la selenocisteína requiere más investigación para comprender plenamente las implicaciones asociadas a su generación celular. Es muy posible que la mayor toxicidad de los análogos sintetizados químicamente se deba a un aumento de los ciclos redox y/o a una mayor inducción de la proteotoxicidad debida a una mayor síntesis de selenocisteína a nivel celular, lo que conduce a una toxicidad oral aguda de impacto similar a la del selenito sódico inorgánico.
La levadura de selenio tiene una toxicidad mucho menor
Un beneficio que aporta la levadura de selenio orgánico en este sentido es la influencia estabilizadora que proporciona la incorporación de selenio en péptidos y proteínas. Al incorporar el selenio a los péptidos y las proteínas en lugar de a los aminoácidos, se reduce enormemente el potencial de inestabilidad
De manera significativa, se anula el impacto sobre el daño del ADN, las proteínas y los lípidos mediado por las ROS a nivel celular. Por el contrario, las fuentes de síntesis química no tienen el beneficio protector de la incorporación de la proteína de la levadura y se ha demostrado que tienen impactos celulares negativos
La inestabilidad de los selenoaminoácidos sintéticos está bien documentada. Por ejemplo, estudios más antiguos, que ponen de relieve este fenómeno, sometieron muestras de L-selenometionina sintética y de levadura de selenio orgánico a condiciones de oxidación en forma de desafío de peróxido
Figura 2 – El efecto de las condiciones de oxidación en la recuperación de L-SeMet sintético y SeMet unido a péptidos (levadura de selenio).
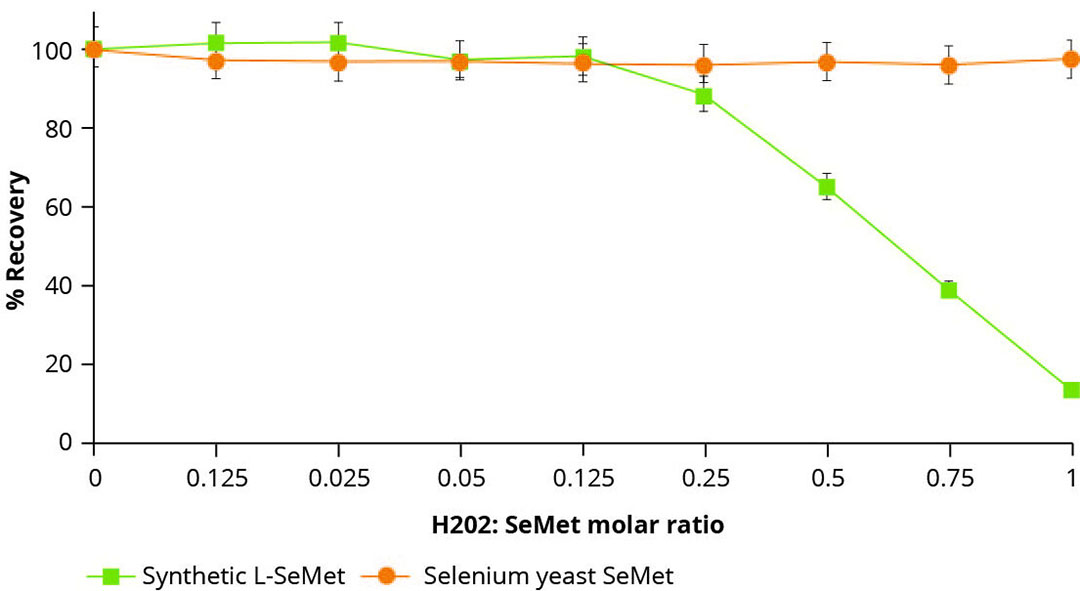
Estos resultados se ilustran en la figura 2, según la cual, al aumentar las condiciones de oxidación de la solución, la recuperación de la L-selenometionina sintética en su forma pura disminuye rápidamente. Por el contrario, la recuperación de selenometionina a partir de la levadura de selenio orgánico se mantuvo constante en las mismas condiciones, lo que ilustra su mayor estabilidad y su menor susceptibilidad a la oxidación. Aunque no se trata de una medición directain vivo, esta sencilla técnica puede ser útil para indicar la estabilidad o inestabilidad potencial de las formas de oligoelementos en un entorno oxidante.
Figura 3 – Efecto de la suplementación con selenio sobre los marcadores de daño al ADN
. SD: deficiencia de selenio, SM: Se sintetizado químicamente. SS: selenito de sodio, YS: levadura de selenio. Los valores con letras diferentes indican diferencias estadísticamente significativas (P<0,05).
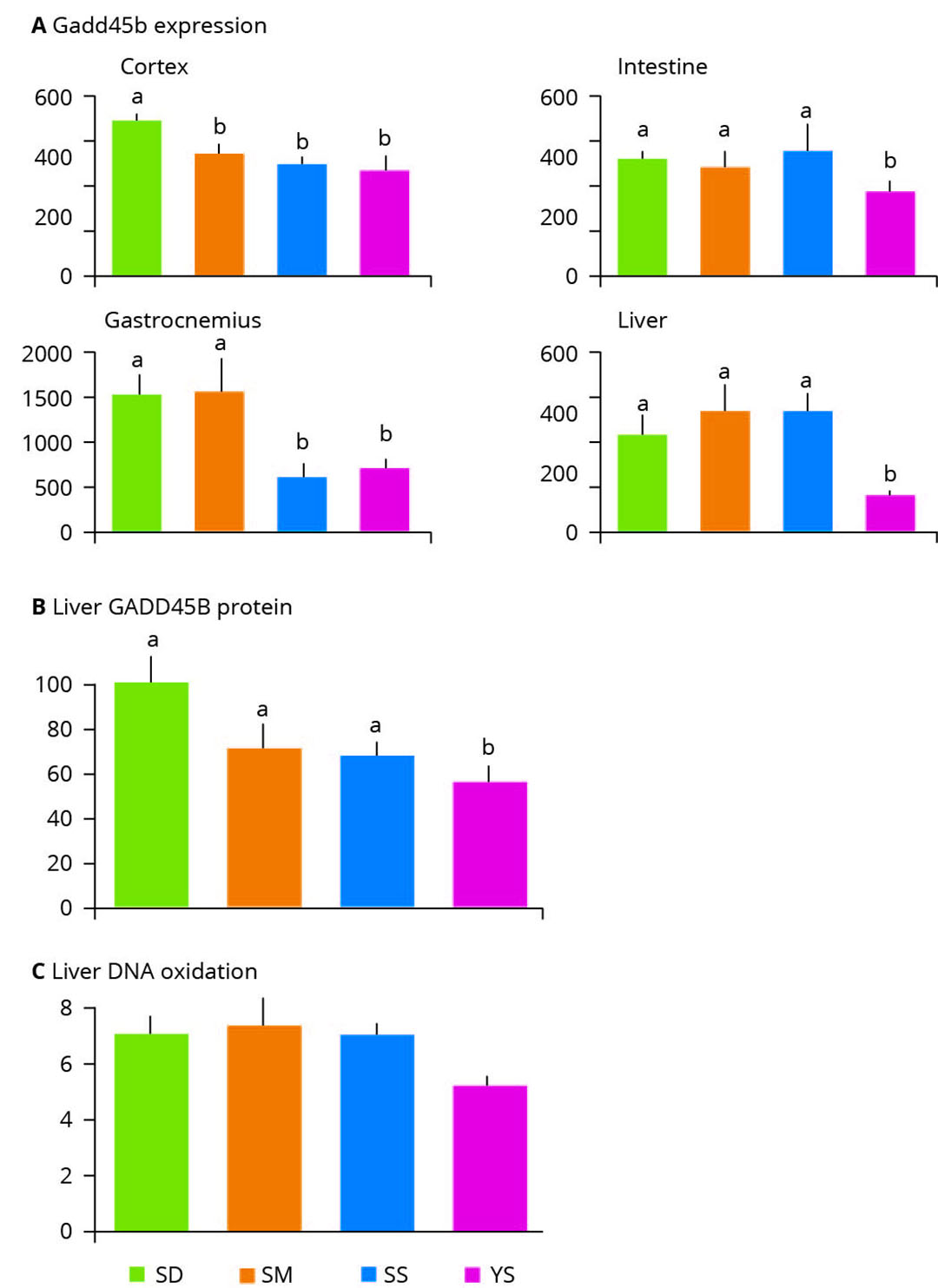
Antioxidante frente a prooxidante
El objetivo principal de añadir selenio a la dieta es proteger contra el estrés oxidativo. El principal resultado del estrés oxidativo, o inducido por los radicales de oxígeno, es el daño al ADN. Una investigación que evaluó los efectos diferenciales del selenito sódico, la L-selenometionina sintética y la levadura de selenio sobre la expresión génica en un modelo animal, arrojó algunos resultados notables. Los autores examinaron la inducción de genes y proteínas relacionados con el daño del ADN, además de los marcadores físicos del estrés oxidativo(Figura 3). Descubrieron que la expresión del gen de respuesta al daño del ADN Gadd45b disminuía sistemáticamente su expresión en todos los tejidos tras la suplementación con levadura de selenio orgánico(Figura 3A). El selenito sódico inorgánico redujo la expresión de Gadd45b en la corteza y el gastrocnemio y la fuente de selenio sintético fue limitada en cuanto a los beneficios celulares y sólo redujo su expresión en la corteza (Figura 3A)
Los autores también observaron que en el hígado, la levadura de selenio redujo significativamente la abundancia de la proteína codificada por el gen Gadd45b, lo que demuestra el impacto protector de la levadura de selenio y contrasta con la incapacidad de las fuentes de selenio inorgánico y sintetizado para hacerlo(Figura 3B). Además, los autores midieron los niveles de un marcador de daño oxidativo del ADN (8-oxo-dG) en el hígado y encontraron una reducción del 27% de 8-oxo-dG en los animales suplementados con levadura de selenio, indicando de nuevo los beneficios protectores de la levadura de selenio(Figura 3C)
Figura 4 – Expresión del oncogén tumoral p53 SD: deficiencia de selenio. SM: Se sintetizado químicamente. SS: selenito de sodio. YS: levadura de selenio.
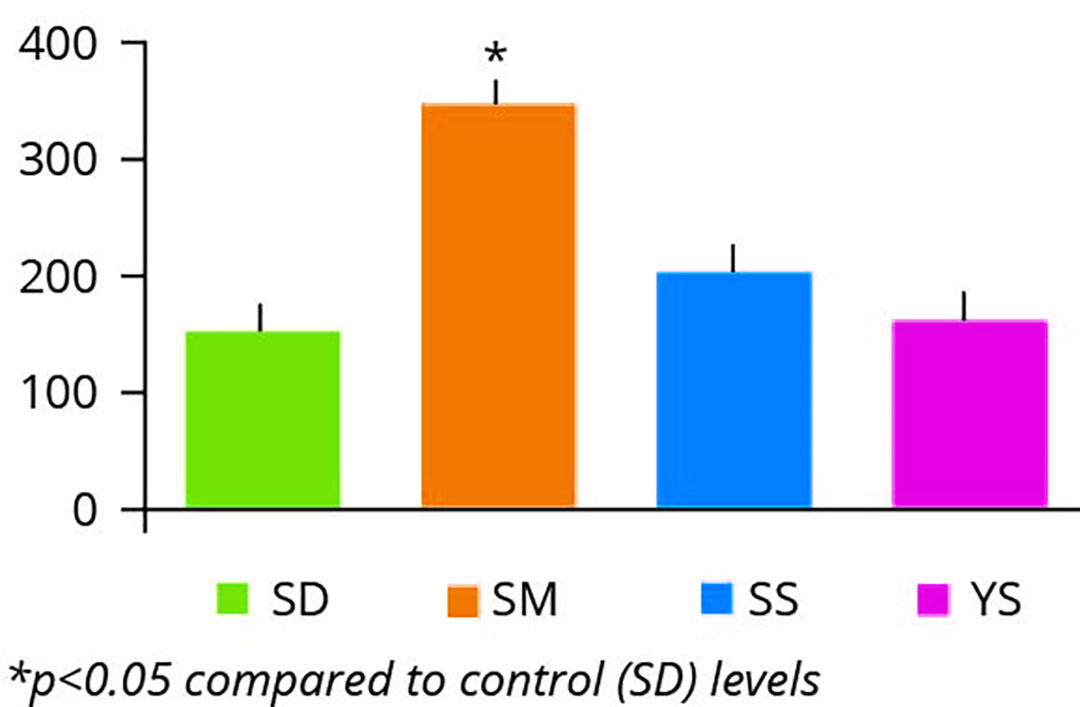
Quizás el hallazgo adicional más sorprendente de este estudio fue la marcada inducción del gen p53 en el tejido intestinal de los animales alimentados con dietas que contenían la fuente de selenio sintetizada químicamente(Figura 4)
Está bien documentado que el gen supresor de tumores p53, un factor de transcripción que controla la respuesta celular al daño del ADN, se induce en la respuesta celular aguda al daño del ADN y también en respuesta al daño crónico y aumentado que se observa en los tejidos envejecidos. Por tanto, el nivel de expresión de p53 sirve como indicador de los niveles endógenos de inestabilidad genómica. Esto sugiere que la fuente de selenio sintético, a diferencia de la levadura de selenio, promueve la genotoxicidad intestinal, lo que podría ser un reflejo de los datos de toxicidad oral aguda destacados en la Tabla 2
En el contexto de los datos globales, está claro que la biodisponibilidad de los selenoaminoácidos y las selenoproteínas variará entre las fuentes a medida que transitan por el tracto gastrointestinal. A un nivel más simplista, también cabe esperar que las diferencias en la estabilidad de las fuentes de selenio afecten a parámetros como la vida útil y la calidad del producto
Y lo que es más importante, estas diferencias pueden influir en el potencial tóxico de los distintos preparados y, en el caso de las fuentes de selenio sintetizadas químicamente, impartir una toxicidad similar a la del selenito sódico inorgánico.
Conclusiones
-
Las diferencias en las fuentes de selenio tienen implicaciones en el rendimiento de los productos que van desde la vida útil y la toxicología hasta la respuesta de los animales.
Pueden demostrarse claras diferencias en las estabilidades relativas de los productos de selenio a nivel de producto, premezcla y alimento.
En comparación con la levadura de selenio, la selenometionina sintetizada químicamente era relativamente inestable y tenía un potencial celular limitado en cuanto a la promoción de una respuesta antioxidante.
El funcionamiento antioxidante puede verse comprometido tras la exposición a altos niveles de selenio sintetizado químicamente.
Esto puede dar lugar a una alteración de los patrones de expresión génica que conduzca a un estrés oxidativo y a alteraciones de la función celular, además de a citotoxicidad y proteotoxicidad. -
Referencias disponibles a petición.
-
Autor:
Richard Murphy PhD, European Bioscience Centre, Alltech Ireland -
-
-
-
